
上海市食品药品监督管理局关于对提供医疗器械贮存、配送服务企业开展专项检查的通知(2018年7月25日)
沪食药监药械流〔2018〕146号
市食药监局认证审评中心、市食药监局执法总队、各区市场监管局:
为进一步加强本市为其他医疗器械生产经营企业提供贮存、配送服务企业(以下简称“三方物流企业”)的监管,落实企业主体责任,督促本市医疗器械三方物流企业按照《上海市医疗器械经营质量管理规范实施细则》要求开展医疗器械贮存、配送服务,按照《2018年上海市医疗器械监管工作计划》安排,结合本市监管实际,现制定专项检查方案如下:
一、检查对象
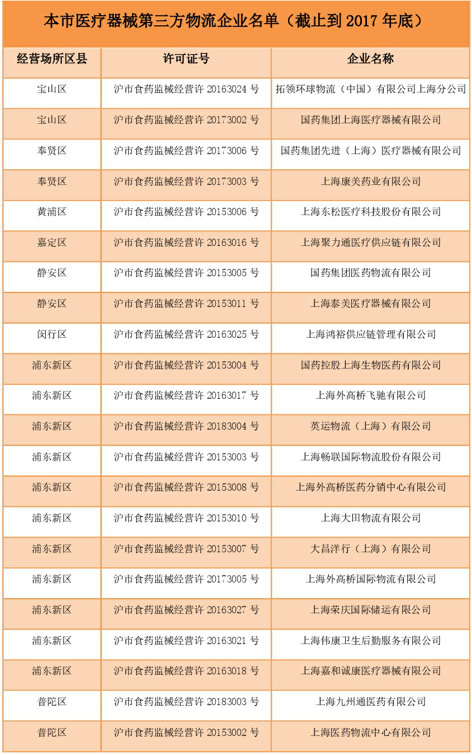
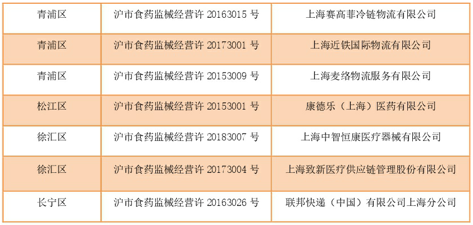
2017年底前取得《医疗器械经营许可证》,且许可证经营范围中包含“为其他医疗器械生产经营企业提供贮存、配送服务”的企业,共31家,截止到目前已经有2家未能按时许可延续,原许可证过期注销(附件1)。
二、检查内容
依据《医疗器械经营质量管理规范》《医疗器械冷链(运输、贮存)管理指南》《上海市医疗器械经营质量管理规范实施细则》中有关要求,重点对三方物流企业实际贮存运输情况是否与许可事项一致,是否按照医疗器械产品标签、标识的要求对产品进行贮存、运输,提供给监管部门的实时监管信息平台是否真实与实际一致,企业自查及发现问题整改落实等执行GSP情况开展核查,本次专项具体检查内容详见《2018年度专项检查表》(附件2)。
检查结论的判断标准以检查项目全部符合要求为“通过检查”,检查项目一项以上(含一项)不符合要求为“限期整改”,现场检查涉嫌违法违规需进一步调查,固定现场证据后,及时予以立案处理。
三、检查安排
(一)检查时间
2017年8月1日―2017年10月31日
(二)工作分工
市食药监局药械流通监管处负责制定总体方案,确定检查企业名单,明确检查要求,制定现场检查表,监督检查结果信息公开以及协调检查期间的相关工作。
市食药监局认证审评中心负责承担组织检查工作,结合日常许可检查安排,制定检查计划,根据企业库房数量、企业规模合理安排检查时间,汇总检查结果及专项总结。
市食药监局执法总队派员参加检查,根据检查安排担任检查组长。围绕企业合法性进行审核,发现违法行为,及时予以立案处理。
区市场监管局派员参加对本辖区内企业的检查。
(三)检查人员组成
检查组由市食药监局认证审评中心、市食药监局执法总队、企业所在区市场监管局各派1人组成,市食药监局药械流通监管处根据工作安排派员参加。
市食药监局认证审评中心根据检查安排,提前一周通知市局执法总队和企业所在地市场监管局,并将检查安排抄告市局药械流通处。
四、检查要求
(一)实行组长负责制。组长做好检查分工和任务安排,认真按照本次专项检查的内容逐一核查,对现场发现的不符合要求的情况进行记录和拍摄,对相关文件资料进行复印,记录检查现场情况、发现的问题等内容,并经检查企业签字确认。检查结果及时录入我局证后监管系统,检查表于检查结束一周内送交市食药监局药械流通处。
(二)检查结果及时处置。对需要限期整改,应当立即报市食药监局药械流通监管处;涉嫌违法违规的,由执法总队立案调查,依法处置。
(三)督促企业整改到位。对检查中发现的缺陷,由市食药监局药械流通监管处向企业发出《限期整改通知书》,企业应当7日内向检查组提交整改报告,并限期完成整改。
(四)严格遵守廉政纪律。在监督检查中,检查组要严格依法行政。检查中文明执法,不接受企业餐饮宴请及车辆接送,杜绝借检查之机收受被检查单位礼金礼品等行为。
特此通知。
附件:
邮政编码:200052 电话:021-63800152 传真:021-63800151 京ICP备15010734号-10 技术:网至普网站建设