【审评报告】寡糖链检测试剂盒(荧光毛细管电泳法)
更新时间:2024/4/28 16:59:11 浏览次数:3586国家药品监督管理局医疗器械技术审评中心于2024年4月25日公开《寡糖链检测试剂盒(荧光毛细管电泳法)》产品注册技术审评报告。申请人:江苏先思达生物科技有限公司。
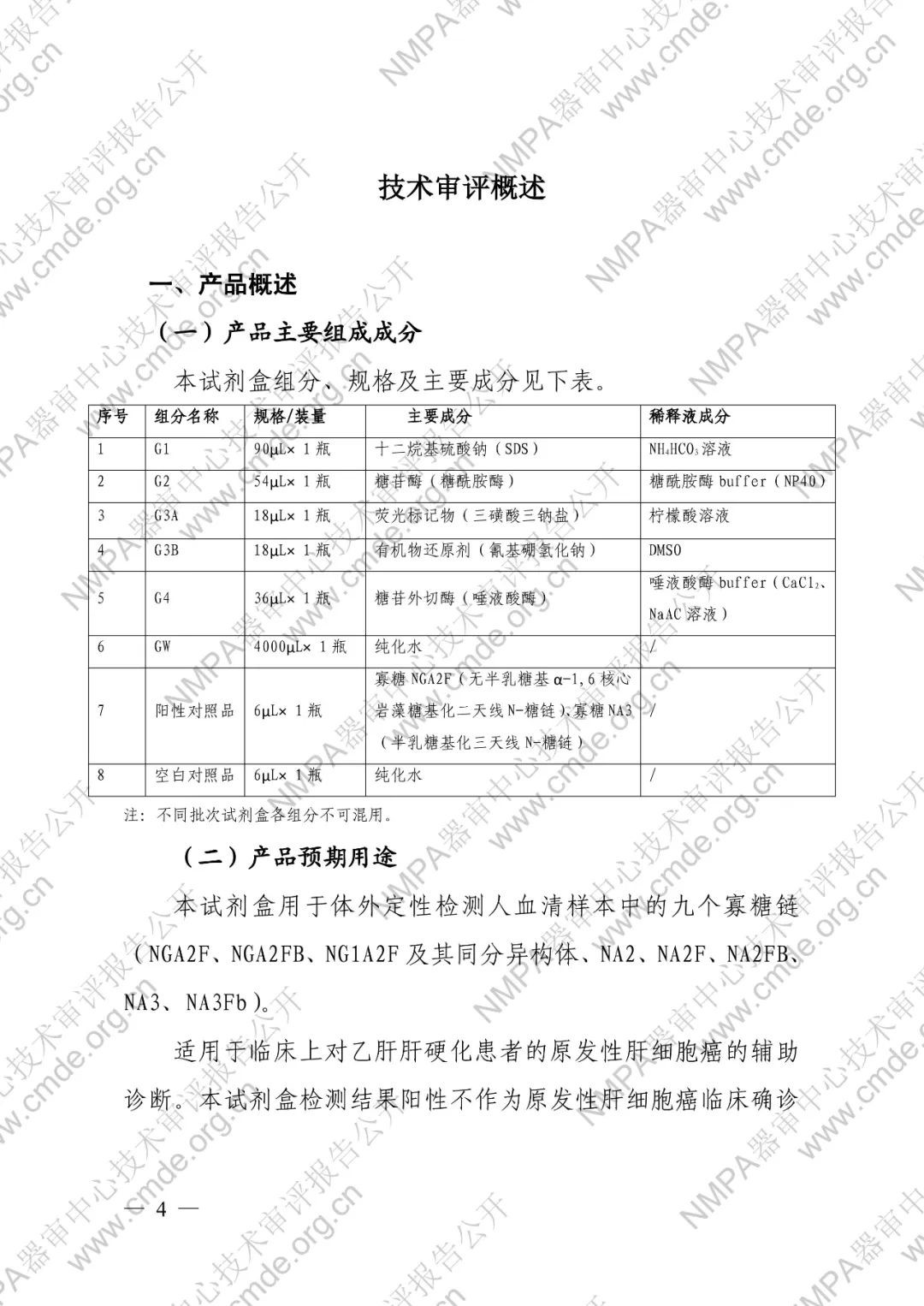
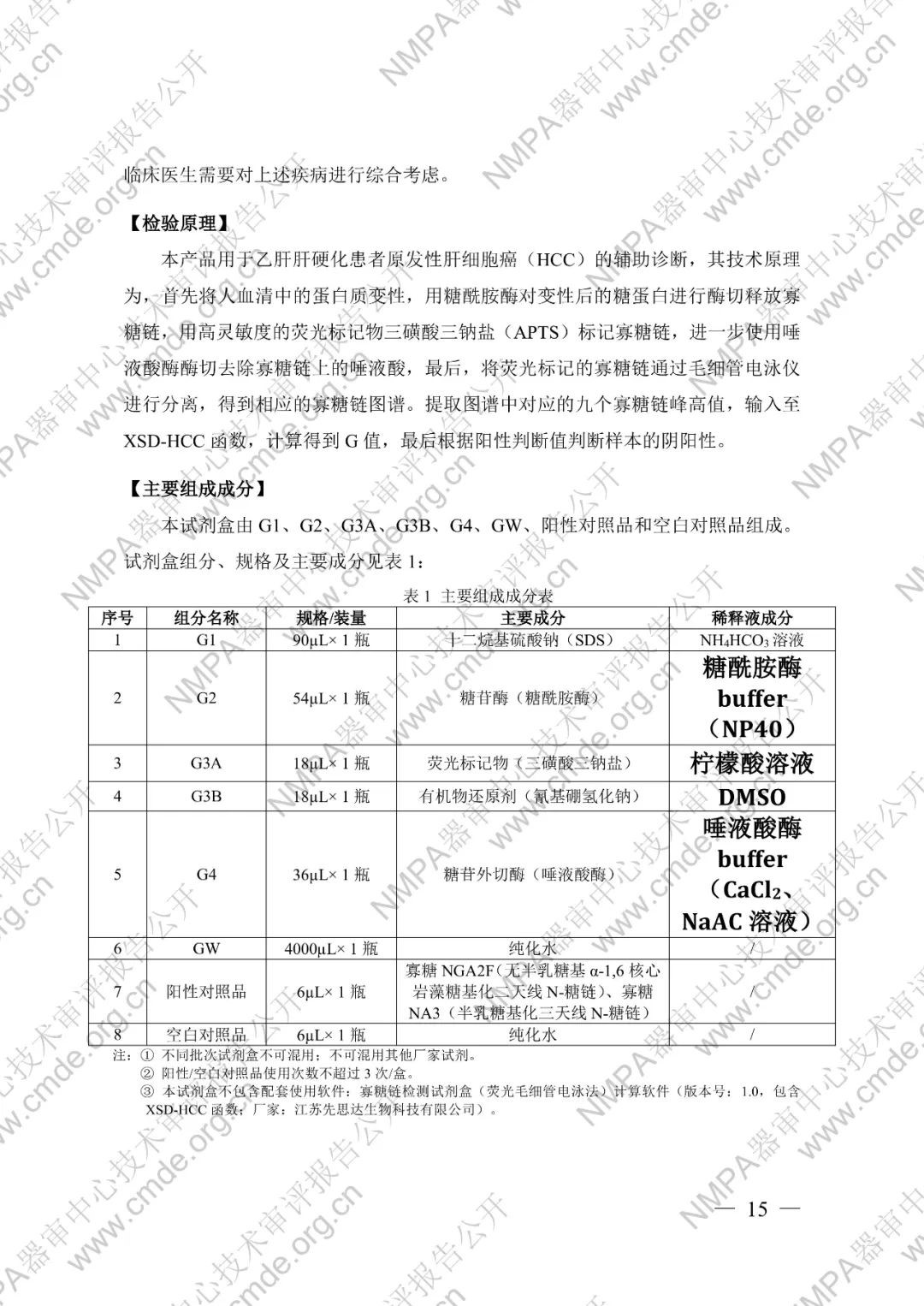
本试剂盒用于体外定性检测人血清样本中的九个寡糖链(NGA2F、NGA2FB、NG1A2F 及其同分异构体、NA2、NA2F、NA2FB、NA3、NA3Fb)。
适用于临床上对乙肝肝硬化患者的原发性肝细胞癌的辅助诊断。本试剂盒检测结果阳性不作为原发性肝细胞癌临床确诊的唯一依据,检测结果阴性也不能排除原发性肝细胞癌的可能。该检测不能作为原发性肝细胞癌确诊的依据,不宜用于普通人群的肿瘤筛查。
本试剂盒对于肝内胆管癌、混合型肝癌也有一定的阳性检出率。本试剂盒对于丙肝肝炎、丙肝肝硬化、丙肝肝癌、肝脓肿、转移性肝癌、食管癌、贲门癌、胃癌、肠癌和肺癌的检测特异性较低,这类疾病患者不适合采用本试剂盒进行检测。当检测结果为阳性时,临床医生需要对上述疾病进行综合考虑。





















来源:NMPA
 扫描下载
扫描下载体外诊断头条APP
 扫描关注
扫描关注CAIVD官方微信
 扫描关注
扫描关注CAIVD官方视频号
 扫描关注
扫描关注CACLP官方微信
 扫描关注
扫描关注CACLP官方视频号
全国卫生产业企业管理协会实验医学分会
( 京ICP备15010734号-10 )



